4.IND創新藥申報情況
IND是指新藥臨床研究審批,新藥的產生需要進行兩次行政審批,一是在臨床研究階段(IND申報),二是臨床研究完成注冊上市(NDA申報)。中國創新藥的研發正處于快速發展的階段,IND數量由2017年的236件增長至2022年的600件,復合年均增長率達20.5%。其中,2021年中國首次IND藥品數量再創歷史新高,國產共有496件,進口共有156件。
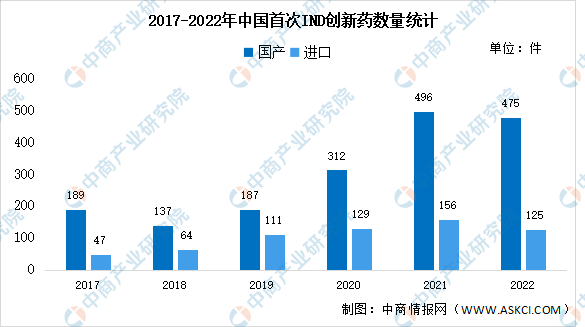
數據來源:醫藥魔方、中商產業研究院整理
2022年,我國首次進行IND申報的新藥數量達600件,其中,國產藥品475件,占比79%。國產創新藥IND申報主要集中于腫瘤、血液以及免疫領域,2022年占比分別為42%、11%、6%。
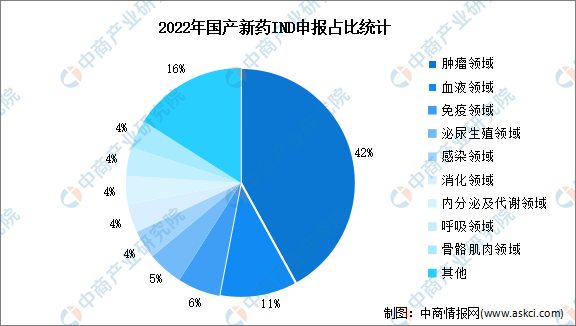
數據來源:醫藥魔方、中商產業研究院整理
5.投融資情況
我國創新藥研發水平與國際的差距正在逐步收窄,我國正在經歷“仿制藥-創新藥”的轉變過程與突破。2023年1-9月,中國創新藥投資事件為5起,投資金額達10.9億元。
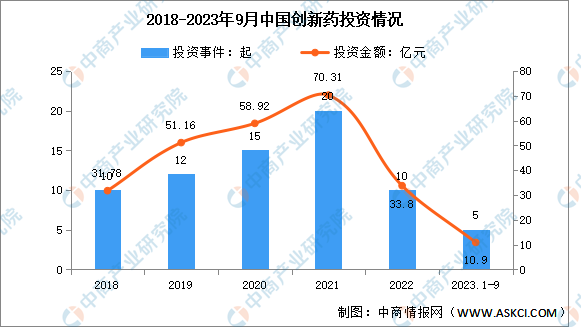
數據來源:IT桔子、中商產業研究院整理
 如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。
如發現本站文章存在版權問題,煩請聯系editor@askci.com我們將及時溝通與處理。

